Síndrome de Vogt Koyanagi Harada
El Síndrome de Vogt Koyanagi Harada (VKH) es una enfermedad crónica de origen desconocido, que tiene manifestaciones oculares con inflamación del tracto uveal, retina, nervio óptico, y manifestaciones extra oculares que afectan el sistema nervioso central y la piel.
Etiología
Se piensa que la misma podría ser el resultado de un proceso autoinmune dirigido contra los melanocitos coroideos, en sujetos genéticamente predispuestos, siendo más común en mujeres. Afecta predominantemente a individuos asiáticos, hispánicos y a la población indio-americana.
Manifestaciones Oculares
Las manifestaciones clínicas se agrupan en 3 períodos o fases.
Comienza en el estadío prodrómico, con cefaleas, zumbidos en los oídos (acúfenos), hipersensibilidad del
cuero cabelludo, dolor de cuello con rigidez de nuca.
Estos síntomas duran unos pocos días para dar lugar al estadío uveítico, que se prolonga semanas a
meses, y se caracteriza por disminución súbita de visión que afecta ambos ojos en 70 % de los casos,
mientras que el 30 % restante experimenta compromiso del segundo ojo hasta 10 días más tarde. La
manifestación más común es un desprendimiento de retina exudativo que en un principio puede estar
acompañado con uveítis anterior, vitreítis, hiperemia y edema del nervio óptico. El desprendimiento de
retina exudativo puede manifestarse como edema de mácula con pliegues retinales o desprendimientos
serosos múltiples localizados, todos ellos producidos por la inflamación y exudación a nivel de
coroides. La inflamación intraocular que se asocia al desprendimiento de retina exudativo puede hacerse
presente varios días después del comienzo de la enfermedad y a veces nunca si el tratamiento es lo
suficientemente precoz.
En el período de convalecencia se hacen presente manifestaciones típicas de la enfermedad que pueden
contribuir al diagnóstico cuando la enfermedad se presenta en forma incompleta. Se produce una
depigmentación del fondo de ojos por afectación difusa del epitelio pigmentario que puede dar el aspecto
de un fondo de ojo albino. Esto se lo denomina “sunset glow fundus”. El epitelio pigmentario puede
también reagruparse y formar acúmulos de pigmento. Además de las alteraciones pigmentarias en el período
de convalecencia aparecen nódulos pequeños, amarillentos y especialmente localizados en el sector
inferior que son similares a los nódulos de Dalen-Fuchs que se ven en la oftalmía simpática.
Reactivaciones
Si el tratamiento es adecuado, la enfermedad se inactiva en un período que varía entre 6 meses y un año,
pero puede haber reactivaciones.
Las reactivaciones tempranas se producen en general por una disminución rápida o suspensión del
tratamiento y consisten principalmente en la reaparición del desprendimiento de retina exudativo.
Las reactivaciones tardías son más comunes y consisten en una uveítis anterior crónica que en ocasiones
no responde al tratamiento con corticoides y es indicación de tratamiento con inmunosupresores.
Complicaciones
La inflamación crónica puede dar origen a complicaciones tales como sinequias posteriores, glaucoma, catarata subcapsular posterior y membranas neovasculares coroideas de localización macular o peripapilar.
Manifestaciones Extraoculares
Las manifestaciones extraoculares tempranas incluyen signos meníngeos y alteraciones del oído interno (hipoacusia de altas frecuencias). Las manifestaciones más tardías son poliosis y vitiligo, que en nuestro medio son poco frecuentes, pero contribuyen en el diagnóstico de VKH.
Diagnóstico
El diagnóstico es clínico y se realiza reconociendo las manifestaciones típicas de la enfermedad. Estudios complementarios como la RFG, OCT y ecografía pueden ser necesarios para complementar los hallazgos clínicos.
Tratamiento
La base del tratamiento consiste en la administración sistémica de corticoides a altas dosis en el
período agudo, y la tendencia actual es combinarla precozmente con inmunosupresores. Con un manejo
adecuado, la inflamación desaparece en aproximadamente 6 semanas y se controla en casi todos los casos
entre los 6 meses y el año. Para ello el tratamiento debe tener tres características fundamentales. Debe
ser: precoz, agresivo y prolongado.
La uveítis anterior asociada debe tratarse con prednisolona tópica al 1 %, ajustando la frecuencia según
la intensidad de la inflamación. También se recomienda el uso de midriáticos y cicloplégicos para
disminuir el espasmo ciliar y prevenir la formación de sinequias posteriores.
Tratamiento quirúrgico
Las complicaciones del VKH como la catarata y glaucoma requieren cirugía. En el primer caso suelo hacer una cirugía combinada de facoemulsificación de la catarata combinada con vitrectomía ya que la vitrectomía mejora el pronóstico de la cirugía de catarata al disminuir la reacción inflamatoria. El glaucoma que no responde a las gotas debe tratarse con la colocación de válvulas de drenaje (válvula de Ahmed).
Imágenes
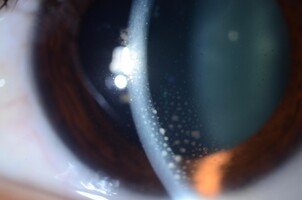

Uveítis anterior.
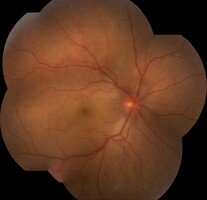
Desprendimiento de retina exudativo.

Desprendimiento de retina exudativo y papilitis.

Alteración difusa del epitelio pigmentario y nódulos coroideos.
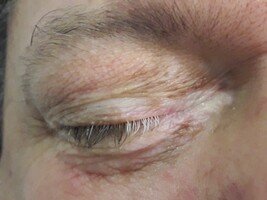
Vitiligo y poliosis como manifestaciones tardías.

Depigmentación difusa (sunset glow fundus).
Toxoplasmosis ocular
La toxoplasmosis ocular es una enfermedad muy común en Argentina y que se manifiesta tanto en personas
sanas como en aquellas que puedan tener alguna alteración de la inmunidad.
Afecta principalmente la retina que es donde se encuentra alojado el parásito y secundariamente otras
estructuras del ojo por reacción inflamatoria: uveítis anterior, vitreítis, vasculitis, papilitis y
coroiditis.
Transmisión
El huésped definitivo del Toxoplasma gondii es el gato, donde se cumple el ciclo evolutivo del parásito
y a partir de allí éste elimina al parásito por la materia fecal.
Una vez eliminado por la materia fecal, el parásito puede contaminar el medio ambiente y a otros
animales.
La ingestión de quistes de tejidos que se encuentran en la carne cruda o mal cocida de diferentes
animales es la principal vía de contagio. La carne de cerdo es la que históricamente se consideraba más
comúnmente responsable de esta vía de contagio.
En Brasil, la carne de pollo es también considerada una forma de transmisión, habiéndose encontrado
resultados positivos en 20-40% de las muestras testeadas.
Existen recomendaciones para poder eliminar al parásito de los tejidos para que sean viables para el
consumo. Congelar la carne a –12 grados C por más de tres días, o cocinar la carne a 67 grados C de
temperatura interna pueden matar a los quistes que se encuentran en los tejidos. Además de la carne de
diferentes animales, las frutas y verduras pueden actuar como vectores para llevar el parásito hasta el
hombre y provocar el contagio de la enfermedad.
Los ooquistes presentes en el suelo, pueden también ser inhalados si se dispersan por el aire.
La transmisión a través del agua ha sido demostrada en diferentes lugares del mundo por la contaminación
del agua potable.
Una de las primeras formas de contagio conocidas fue la vía trans placentaria en la cual la madre en
período de gestación contrae la enfermedad y transmite el parásito al feto a través de la placenta. Esta
forma es la responsable de las manifestaciones características de toxoplasmosis congénita.
Los trasplantes de órganos y la leche no pasteurizada también han sido reportados como causa de contagio
de la toxoplasmosis ocular.
Una vez que el parásito llega al organismo por cualquiera de las vías mencionadas, se generan
anticuerpos IgM primero e IgG después que duran toda la vida. Pero el parásito queda alojado en
diferentes tejidos en forma latente, entre ellos la retina. Estos quistes retinales pueden reactivarse
en cualquier momento de la vida y provocar entonces la conocida toxoplasmosis ocular.
Características oculares
Cuando se rompen estos quistes retinales y el parásito comienza a replicarse se produce una lesión
blanco amarillenta en la retina que es bien característica (retinitis). Esta lesión puede aparecer sola
o asociada a una cicatriz previa que se genera en forma asintomática cuando se produce el contagio
inicial con el parásito.
Además de la retinitis producida por el parásito se desencadena una reacción inflamatoria que puede
afectar múltiples estructuras del ojo. Puede producir uveítis anterior, vitreítis, vasculitis,
papilitis, coroiditis y hasta la misma retina puede estar inflamada.
Formas clínicas de presentación
Existen varios patrones de presentación de la toxoplasmosis ocular que es importante reconocer ya que su
diagnóstico se basa en el reconocimiento de las manifestaciones clínicas:
Toxoplasmosis congénita: se produce cuando la infección materna
ocurre durante el embarazo. La incidencia de infección congénita es menor en el primer trimestre, pero
suele ser más severa. Si la infección es adquirida durante el tercer trimestre, la transmisión al feto
ocurre casi en el 60% de los casos, probablemente debido a una mayor vascularización de la placenta. Se
producen lesiones bilaterales en 85% de los pacientes y afecta la mácula en 58% de ellos. Otras lesiones
que pueden asociarse a la toxoplasmosis congénita son hidrocefalia, microcefalia, convulsiones,
calcificaciones cerebrales, organomegalia, rash y fiebre.
Toxoplasmosis recurrente: es la forma clínica más común de
toxoplasmosis ocular que típicamente se presenta como un foco de retinitis adyacente a una cicatriz
coriorretinal que se produjo como resultado de una infección adquirida previamente.
Afecta a adultos jóvenes de ambos sexos, generalmente en forma unilateral, a pesar que ambos ojos pueden
tener cicatrices coriorretinales. Los títulos de anticuerpos suelen ser bajos debido al lapso
transcurrido entre la primoinfección adquirida tempranamente en la vida y la retinocoroiditis que se
manifiesta tardíamente (75% entre los 10 y 35 años de edad).
Toxoplasmosis primaria: actualmente se considera que la mayor
parte de los casos de toxoplasmosis ocular podrían ser adquiridos en forma postnatal. En esta
presentación se observan lesiones de retinitis en general únicas y sin una cicatriz previa. Pueden estar
o no asociadas con reacción inflamatoria intraocular.
Toxoplasmosis relacionada al SIDA: en estos pacientes con
inmunosupresión variable, se aprecian lesiones en general no tienen cicatriz previa y que pueden ser
bilaterales, difusas y multifocales. Tienen además una mayor asociación con el desarrollo de
toxoplasmosis cerebral.
Toxoplasmosis relacionada con corticoides: en pacientes
inmunocompetentes en los que el tratamiento antiparasitario no es implementado y a su vez reciben
corticoides locales de depósito o sistémicos, pueden desarrollan lesiones extensas similares a las que
se ven en pacientes con SIDA. Nunca hay que dar corticoides en pacientes con toxoplasmosis ocular sin la
cobertura de antibióticos.
Toxoplasmosis relacionada con inmunosupresores: hay pacientes que
por su enfermedad de base deben ser tratados con drogas inmunosupresoras (enfermedades oncológicas o
reumáticas). La toxoplasmosis ocular puede presentarse de manera difusa o con lesiones múltiples,
diferente a lo que habitualmente observamos, con la consiguiente dificultad para reconocerla.
Toxoplasmosis relacionada a la edad: la edad por si misma
constituye un factor de riesgo para tener formas extensas y difusas de toxoplasmosis ocular similar a la
que se observa en los pacientes tratados con corticoides o en inmunosuprimidos. Los mayores de 50 años
suelen tener lesiones de mayor tamaño que aquellos que tienen menos de 50 años de edad.
Toxoplasmosis con obstrucción vascular: la perivasculitis es un
hallazgo frecuente en toxoplasmosis ocular. Este envainamiento puede ocurrir adyacente a un foco de
retinitis o puede ocurrir a distancia. Esta vasculitis puede generar una obstrucción vascular en los
lugares de retinitis activa y es importante reconocer estos cuadros ya que modifican el aspecto típico
de la toxoplasmosis ocular.
Toxoplasmosis con papilitis o neurorretinitis: se trata de un
edema de papila unilateral que se manifiesta como una masa blanquecina inflamatoria adyacente al nervio
óptico.
Conserva buena agudeza visual si la mácula no está comprometida. Esta inflamación del nervio óptico
puede asociarse con una estrella macular simulando una neurorretinitis de otras causas como son la
neurorretinitis idiopática estrellada de Leber o la enfermedad por arañazo de gato.
Diagnóstico
La toxoplasmosis ocular se diagnostica clínicamente.
Como es la forma de uveítis posterior más común en muchos países es bueno considerar que cuando un
paciente adulto joven inmunocompetente se presenta con una retinitis focal asociada o no a una cicatriz
coriorretinal, deberá considerarse que la toxoplasmosis ocular es el diagnóstico más probable.
La serología positiva para toxoplasmosis (IgG e IgM) confirma exposición al parásito Toxoplasma gondii,
pero su positividad no nos confirma un diagnóstico de toxoplasmosis ocular.
Dentro de las pruebas de laboratorio para detectar anticuerpos se encuentra la reacción de
Sabin-Feldman, que es poco utilizada, ya que se necesitan parásitos vivos para realizarla. Las pruebas
que más se utilizan son el test de ELISA o la inmunofluorescencia indirecta (IFI). El test de ELISA
tiene ventajas para detectar IgM mientras que para IgG es similar a la IFI.
La reacción en cadena de la polimerasa (PCR) ha permitido identificar antígenos del parásito en fluidos
oculares sin embargo su sensibilidad y especificidad aún es baja en muestras de humor acuoso y deben
tomarse muestras del humor vítreo. Por lo tanto, su utilidad en el diagnóstico de toxoplasmosis ocular
es limitado.
Tratamiento
El tratamiento de toxoplasmosis se realiza combinando antibióticos para eliminar al parásito que esta
activo y corticoides para eliminar la reacción inflamatoria asociada.
Existen múltiples esquemas desde el tratamiento clásico con pirimetamina y sulfadiacina; la combinación
de pirimetamina y azitromicina, la asociación de trimetoprima y sulfametoxazol; y la clindamicina ya sea
por vía oral o como inyecciones intravítreas. Todas estas opciones deben ir acompañadas de corticoides
para eliminar la reacción inflamatoria.
Imágenes
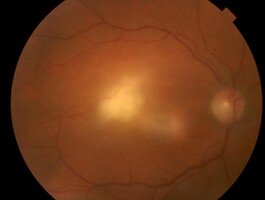
Toxoplasmosis recurrente con retinitis adyacente a una cicatriz previa.

Toxoplasmosis primaria sin cicatriz previa.
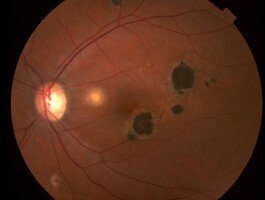
Toxoplasmosis congénita con lesiones múltiples.
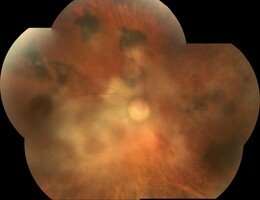
Retinitis difusa asociada al SIDA.

Neuroretinitis por toxoplasmosis.

Toxoplasmosis difusa asociado a la edad.